脳深部刺激療法(deep brain stimulation:DBS)
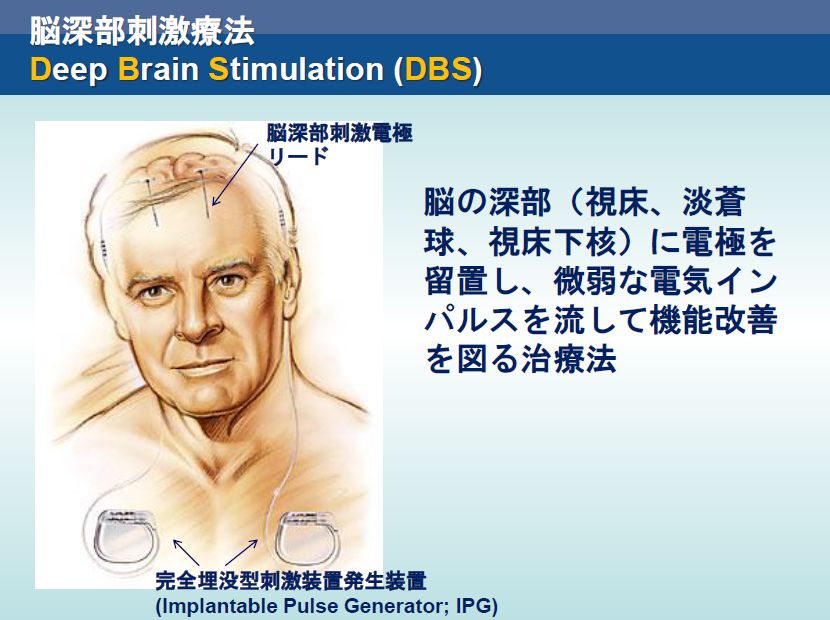 DBSは機能異常をきたしている中枢神経系疾患に対して、脳内に深部電極を留置し、標的を電気刺激することにより、異常な神経活動を制御する治療法です。
DBSは機能異常をきたしている中枢神経系疾患に対して、脳内に深部電極を留置し、標的を電気刺激することにより、異常な神経活動を制御する治療法です。
この治療の特徴は、1)刺激部位における組織の損傷をほとんどきたすことなく、2)刺激条件や刺激部位を変更することで症状の変化に合わせて調整が可能であり、刺激による副作用を軽減させることができる。3)刺激を中止することで、元の状態に戻すことが可能である。そのため、治療のやり直しも行うことができる。このようにDBSは「安全性」「調節性」「可逆性」の面で大変優れた治療法であります。
わが国では、2000年にパーキンソン病と本態性振戦に対して保険収載されており、主に不随意運動症に対する外科的治療として普及しています。
DBSが効果を発揮するメカニズムについては完全には解明されていません。DBSが標的部位の神経活動を抑制する、あるいは異常な神経活動パターンが正常化するといわれています。
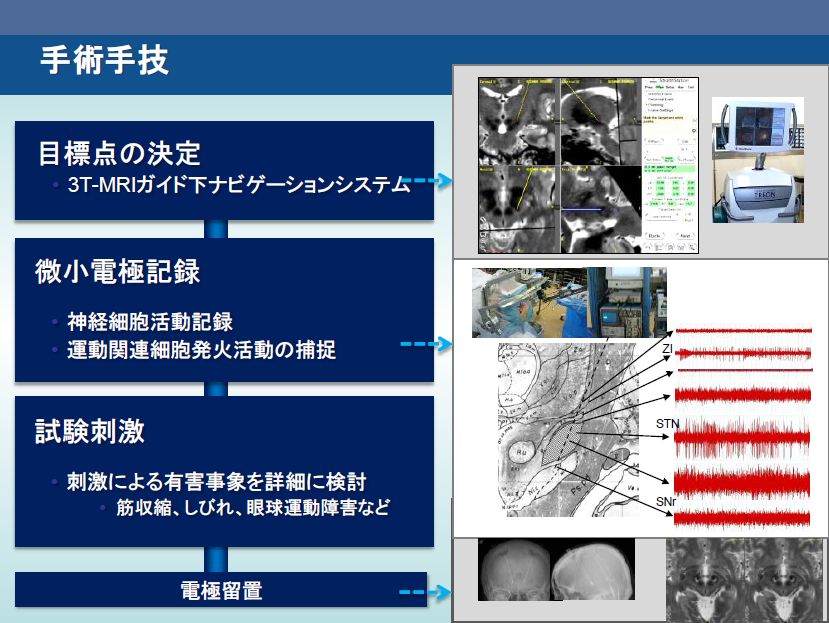
DBSの手術手技
脳深部刺激電極リードの留置は、基本的には定位脳手術装置を用いて行うが、正確で確実な手技が要求されており、手術の成否には次の3プロセスが重要である。
- 標的の決定
MRI、CTなどの画像より、定位脳手術専用ソフトを用いて標的の座標を算出するもので、従来、解剖学的な位置関係に基づき、前交連-後交連を結ぶラインからの距離を基に間接的に算出していたが、高解像度MRIの登場により直接的に標的設定が可能となり、手術精度がより向上している。 - 微小電位記録
電極定位脳装置を用いて標的に微小電極針を挿入して、細胞外活動電位を記録し、標的の神経活動や、受動運動や、感覚刺激に対する神経活動の変化を測定することで、神経生理学的に評価を行う。 - 試験刺激による効果判定
脳深部電極リードを留置し、電気刺激を行い、症状改善の有無や、刺激による副作用の出現状況を評価する。
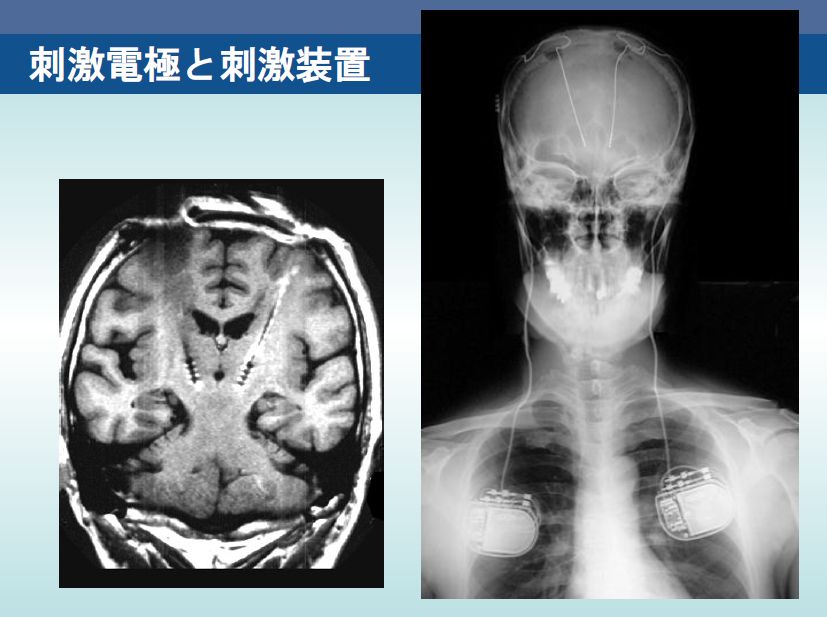 IPGは脳深部電極リードに延長コードを介して接続し、皮下を通して、前胸部や側胸部の皮下に埋没させて設置する。手術後は専用のプログラマーを用いて、体外からIPGに信号を送り、刺激条件や刺激部位の変更を行う。患者自身も患者用プログラマーを持ち、刺激状況の確認や刺激のオン・オフなど制限された範囲であるが、調整が可能である。
IPGは脳深部電極リードに延長コードを介して接続し、皮下を通して、前胸部や側胸部の皮下に埋没させて設置する。手術後は専用のプログラマーを用いて、体外からIPGに信号を送り、刺激条件や刺激部位の変更を行う。患者自身も患者用プログラマーを持ち、刺激状況の確認や刺激のオン・オフなど制限された範囲であるが、調整が可能である。
パーキンソン病に対するDBS
パーキンソン病に対するDBSは、十分な薬物治療を行っても著明なwearing-off現象や、ジスキネジアがコントロールできない症例、薬剤の副作用のために薬物治療が困難な症例、薬剤治療抵抗性の振戦に対して適応となります。

Wearing-off現象に対する効果としては、L-dopaに対する反応性がどれだけ保たれているかが最も重要な要素です。一般には若年者で、L-dopaに対する反応が良い人ほど、良好な手術成績が期待されます。年齢は70歳未満がよいとする意見があるが、高齢者においてもL-dopaに対する反応性がよければDBSの成績もよいので、手術合併症のリスクを個々の症例で評価し、慎重な患者選択を行っております。著しい認知機能低下や精神疾患を合併した人では適応除外となります。
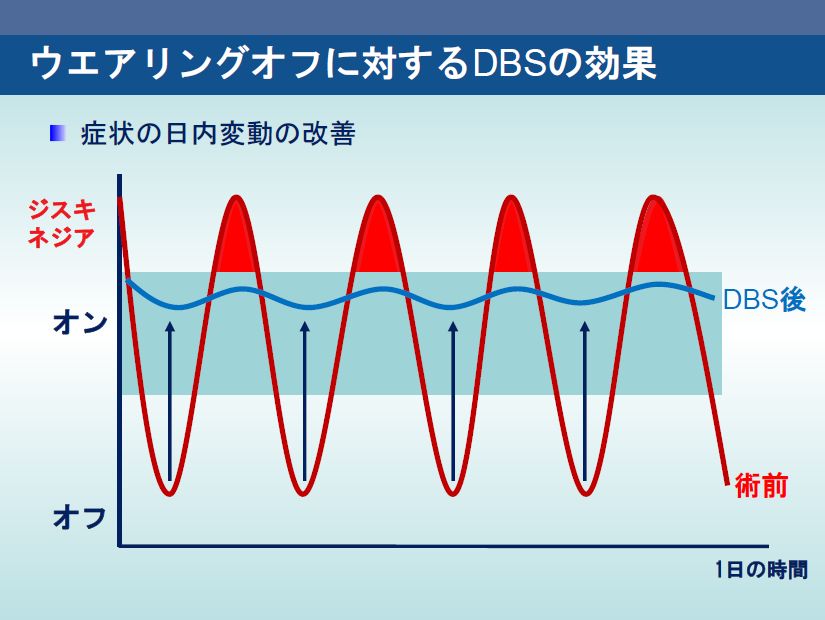
DBSの効果の特徴としては、薬物off時の全ての運動症状の改善やADLの改善です。症状の日内変動が消失することで、患者さんは薬物on時の状態を維持することが可能になります。DBSの効果に関してはエビデンスレベルの高い報告があり、German Parkinson Study Groupによる薬物治療単独群とSTN-DBS併用治療群とに分けた156症例の多施設ランダム化比較試験では、術6か月後、STN-DBS治療群において薬物off時のUPDRS motorスコアの改善、off時間の改善、QOLの改善が有意に認められています。
Kleiner-Fismanらの37前向き研究を含む921症例のシステマティックレビューでは、UPDRSのADLスコアと運動スコアが、術後の薬物off ・刺激on時と術前の薬物off 時との比較において、それぞれ50%、52%改善しました。レボドパ投与量、ジスキネジア、日中のoff時間は術後それぞれ55.9%、69.1%、68.2%減少しております。
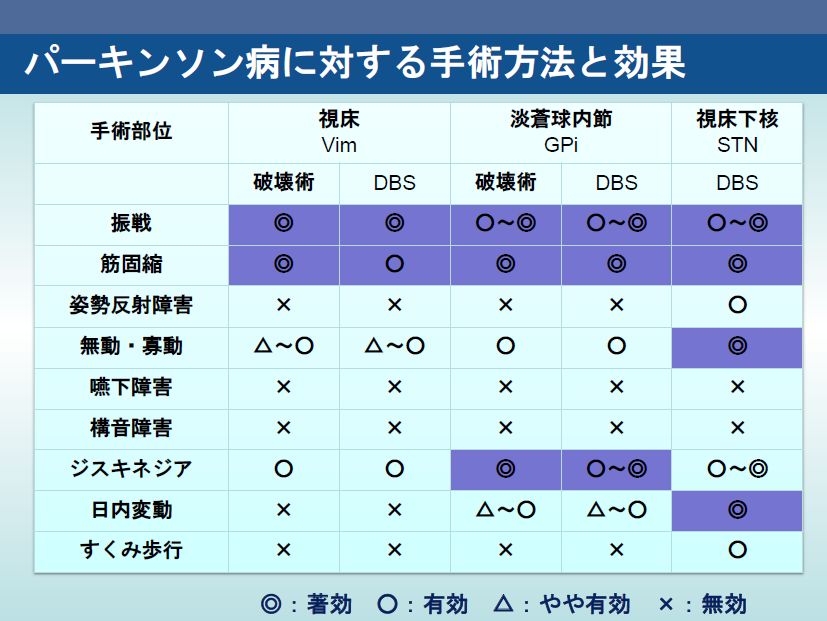
電気刺激を行う部位に関して、STN-DBS(視床下核電気刺激)とGPi-DBS(淡蒼球内節電気刺激)との運動症状に対する効果の違いについては、最近の報告では有効性にはほとんど差は認められていません。STN-DBSでは薬物減量が可能であり、それに伴い薬剤誘発性ジスキネジアの改善が得られる。一方、GPi-DBSでは薬物減量はできないが、薬剤誘発性ジスキネジアに対しては直接的な抑制効果がみられる。視床腹側中間核刺激(Vim-DBS)は、wearing-offに対する効果は期待できないが、振戦に対して強力な抑制効果を有しており、これら臨床効果の違いから個々の症例に合った標的選択を行っております。
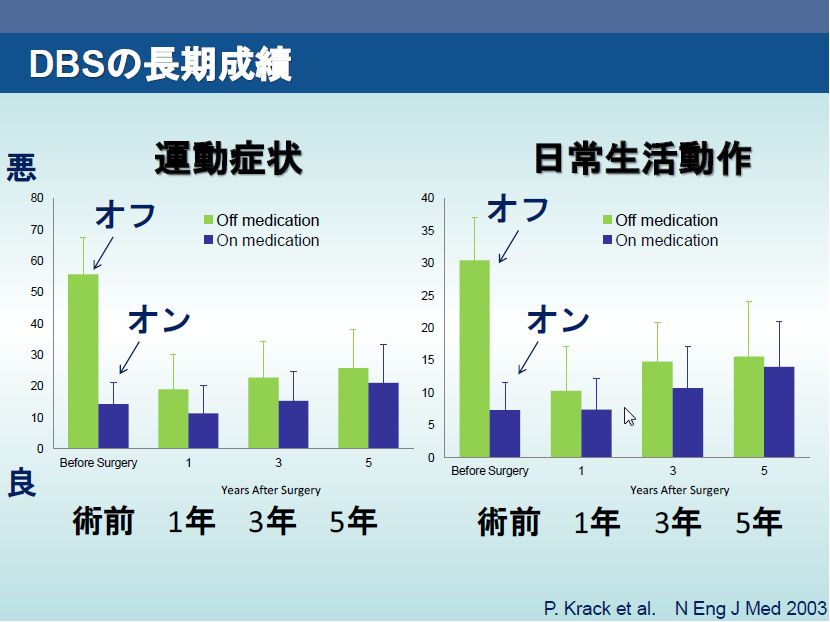
 長期効果ついては、5年間のfollow-upによる二つの大きな前向き研究があり、薬物off時の振戦、固縮、寡動について改善が維持され、レボドパ投与量も減少したままでありました。DBSのパーキンソン病運動症状に対する効果は長期的にも維持されています。
長期効果ついては、5年間のfollow-upによる二つの大きな前向き研究があり、薬物off時の振戦、固縮、寡動について改善が維持され、レボドパ投与量も減少したままでありました。DBSのパーキンソン病運動症状に対する効果は長期的にも維持されています。
 DBSの薬物off時の運動症状改善は効果が高いものの、薬物on時においてはL-dopaの効果を超えるものではありません。またDBSが運動症状に対して、L-dopaとほぼ同等の効果を有する一方で、L-dopa耐性症状に対してはL-dopa同様に効果が減弱してしまいます。進行期において構音障害、歩行時のすくみ、姿勢反射障害などL-dopa耐性症状が前面に出現するような場合、DBSの効果も不十分となります。また、非運動症状に関しては、一部の非運動症状(睡眠異常、薬物off時の疼痛)の改善は認めるものの、通常非運動症状に対する効果は乏しいです。術後L-dopaの過度の減量により、うつやアパシーなどをきたしやすく、これらは一過性であることが多いですが、QOL低下の原因になるため、薬物治療とDBSの微妙なバランスを保ちながら慎重に調整する必要があります。
DBSの薬物off時の運動症状改善は効果が高いものの、薬物on時においてはL-dopaの効果を超えるものではありません。またDBSが運動症状に対して、L-dopaとほぼ同等の効果を有する一方で、L-dopa耐性症状に対してはL-dopa同様に効果が減弱してしまいます。進行期において構音障害、歩行時のすくみ、姿勢反射障害などL-dopa耐性症状が前面に出現するような場合、DBSの効果も不十分となります。また、非運動症状に関しては、一部の非運動症状(睡眠異常、薬物off時の疼痛)の改善は認めるものの、通常非運動症状に対する効果は乏しいです。術後L-dopaの過度の減量により、うつやアパシーなどをきたしやすく、これらは一過性であることが多いですが、QOL低下の原因になるため、薬物治療とDBSの微妙なバランスを保ちながら慎重に調整する必要があります。


パーキンソン病に対する電気刺激療法の流れ
入院期間は2回に分けて行います。第1回目の入院で手術適応の判定と手術方法を決定します。第2回目の入院で手術を行います。入院期間は第1回目が約1週間、第2回目が2〜3週間です。

